Un ensayo en etapa intermedia muestra que una vacuna contra el COVID fabricada en China parece ser segura, según un estudio publicado recientemente en la revista científica Lancet Infectious Diseases.
Sinovac, la compañía china que fabrica la vacuna candidata Coronavac, la probó en un ensayo controlado aleatorio en el que participaron 700 adultos voluntarios sanos entre abril y mayo. Ninguno de los voluntarios tenía antecedentes de infección por COVID-19.
Los voluntarios del ensayo de Fase 2 se dividieron en tres grupos. Un grupo recibió una dosis baja de la vacuna, otro recibió una dosis más alta y un tercero recibió un placebo.
 Osinsa
Osinsa
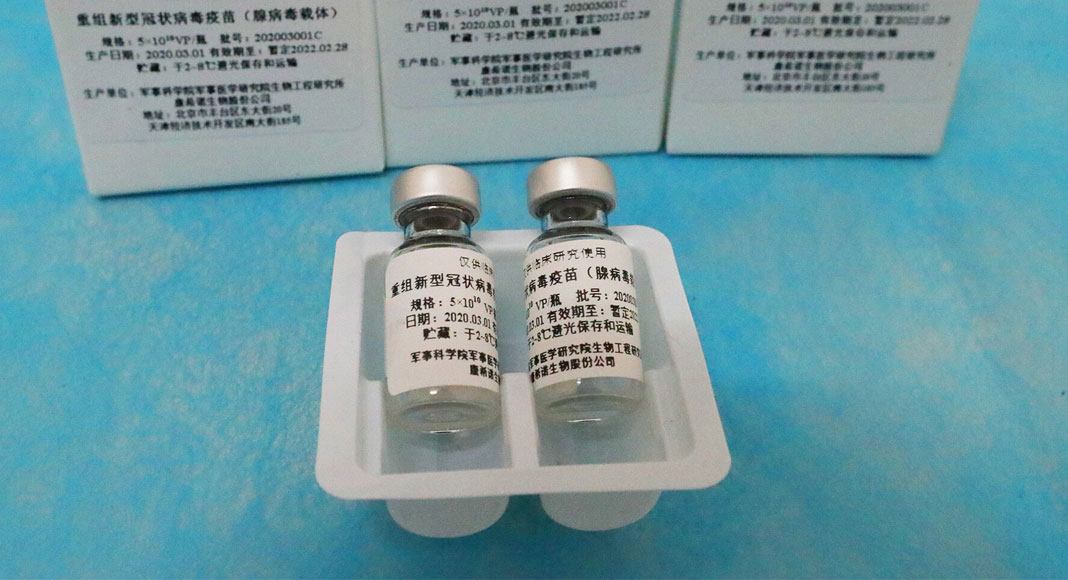
Esta vacuna en particular utiliza un virus completo químicamente inactivado basado en una muestra tomada de un paciente en China. La mayoría de las otras vacunas contra el coronavirus en desarrollo utilizan enfoques biotecnológicos para producir solo un fragmento del virus.
El virus muerto completo es un método antiguo, probado y verdadero que ralentiza la producción de vacunas y que, según los médicos, produce más efectos secundarios.
La vacuna fue bien tolerada en todos los niveles de dosis y no parecía haber ningún problema de seguridad, según los investigadores, expertos del Centro Provincial de Control y Prevención de Enfermedades de Jiangsu, los Institutos Nacionales para el Control de Alimentos y Medicamentos de China y Sinovac.
 Ámbito
Ámbito
La queja más común fue el dolor en el lugar de la inyección. Un voluntario en el grupo de dosis alta tuvo una reacción alérgica grave dentro de las 48 horas posteriores a la primera dosis, que según los investigadores podría estar relacionada con la vacuna, pero el voluntario fue tratado por la reacción y se recuperó en tres días. El mismo voluntario no tuvo una reacción alérgica similar en la segunda dosis.
Incluso con la dosis más baja, los voluntarios que recibieron la vacuna parecieron mostrar una sólida respuesta de anticuerpos dentro de los 14 días posteriores a la segunda de dos inyecciones. Las inyecciones se administraron con un intervalo de 14 días.
 APNews
APNews